Алкены
Алкены – углеводороды, содержащие в своей молекуле одну двойную связь. Также могут быть классифицированы как ненасыщенные углеводороды (наравне с алкинами и алкадиенами).
Общая формула: CnH2n.
Гибридизация
Атомы углерода при двойной связи находятся в состоянии sp2-гибридизации, остальные атомы углерода находятся в состоянии sp3-гибридизации.
Виды изомерии: изомерия цепи, изомерия положения двойной связи, межклассовая изомерия с циклоалканами, цис-транс-изомерия.
Номенклатура
Название алкенов образуется из названия алкильного радикала с суффиксом -ен.
Физические свойства
Физические свойства алкенов практически не отличаются от таковых у соответствующих алканов. Низшие алкены (C2–C4) – газы при нормальных условиях, средние (до C17) – жидкие, высшие являются твердыми веществами. Все алкены нерастворимы в воде и хорошо растворяются в органических растворителях.
Химические свойства
За счет электронов p-связи в молекулах алкенов имеется область повышенной электронной плотности (облако p-электронов над и под плоскостью молекулы). Поэтому двойная связь склонна подвергаться атаке электрофильным (электронодефицитным) реагентом. В этом случае будет происходить гетеролический разрыв связей и реакция пойдет по ионному механизму как электрофильное присоединение.
С другой стороны, углерод-углеродная p-связь, являясь неполярной, может разрываться гомолитически, и тогда реакция будет идти по радикальному механизму.
Для алкенов наиболее характерны реакции присоединения по двойной связи.
Присоединение галогенов по двойной связи С=С происходит легко в обычных условиях (при комнатной температуре, без катализатора). Например, быстрое обесцвечивание синей окраски раствора брома в воде (бромной воды) служит качественной реакцией на наличие двойной связи. Эти реакции протекают по механизму электрофильного присоединения с гетеролитическим разрывом связей в молекуле галогена.
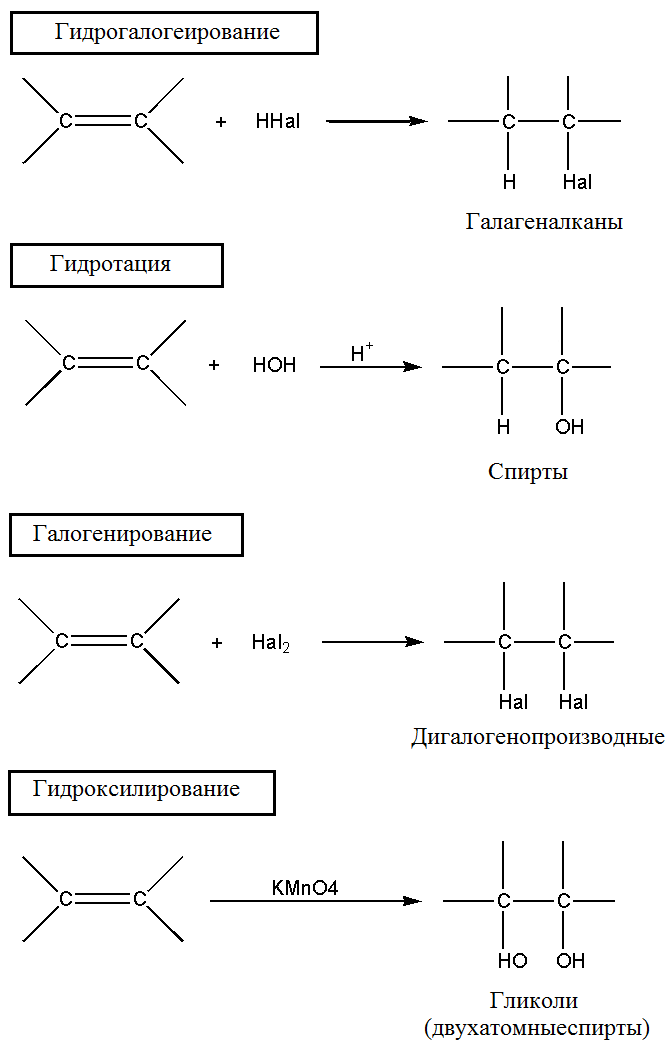
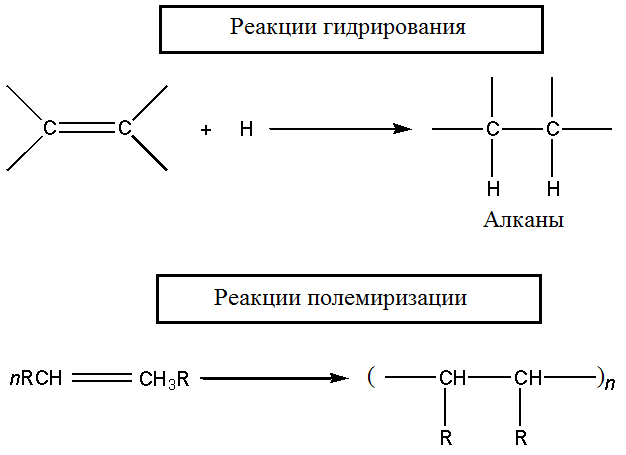
Окисление алкенов
Мягкое окисление алкенов водным раствором перманганата калия приводит к образованию двухатомных спиртов (реакция Вагнера).
В ходе этой реакции происходит обесцвечивание фиолетовой окраски водного раствора KMnO4, поэтому она используется как качественная реакция на алкены. Также возможно окисление до спиртов, альдегидов, кислот, а также полное окисление до углекислого газа и воды (горение).