Определения
Сложные эфиры – органические соединения, производные карбоновых, в которых гидроксильная группа –OH кислотной функции заменена на спиртовой остаток.
Жиры – сложные эфиры глицерина и высших одноосновных карбоновых кислот.
Хлорангидри́д – производное карбоновой кислоты, в которой гидроксильная группа –OH в карбоксильной группе –COOH заменена на атом хлора.
Ангидриды карбоновых кислот – можно рассматривать как продукт конденсации двух групп –COOH.
Амиды – производные кислот, в молекулах которых гидроксильная группа OH замещена на аминогруппу NH2.
Оксикислоты (оксикарбоновые кислоты) – карбоновые кислоты, в которых одновременно содержатся карбоксильная и гидроксильная группы (например, молочная кислота: СН3–СН(ОН)–СООН).
Аминокисло́ты (аминокарбо́новые кисло́ты) – органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. Это строительные блоки, из которых строятся белковые структуры живых организмов.
Кетокислоты – это карбоновые кислоты, содержащие помимо карбоксильной группы –COOH ещё и карбонильную группу =CO. Примерами кетокислот являются пировиноградная кислота. Она является конечным продуктом метаболизма глюкозы в процессе гликолиза. Кетокислоты обладают химическими свойствами как кетонов, так и карбоновых кислот.
Сложные эфиры
Номенклатура и классификация
Название создается следующим образом: вначале указывается группа R, присоединенная к кислоте, затем – название кислоты с суффиксом -ат (например, бутилпропионат).
Строение и физические свойства
Эфиры низших карбоновых кислот и низших одноатомных спиртов имеют приятный запах цветов, ягод и фруктов. Эфиры высших одноосновных кислот и высших одноатомных спиртов – основа природных восков. Например, пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат):
CH3(CH2)14–CO–O–(CH2)29CH3
Химические свойства
Гидролиз эфиров сложных протекает как в кислой, так и в щелочной среде (водные или спиртовые растворы NaOH, КОН):
C2H5COOH + CH3OH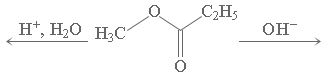 C2H5COO– + CH3OH.
C2H5COO– + CH3OH.
Эфиры сложные устойчивы к действию окислителей.
Восстановление сложных эфиров приводит к альдегидам, но обычно восстановление идет дальше – до первичного спирта:
RCOOR'  RCH2OH + R'OH.
RCH2OH + R'OH.
Методы получения
Получают сложные эфиры: этерификация – взаимодействие кислот и спиртов в условиях кислотного катализа (например, получение этилацетата из уксусной кислоты и этилового спирта):
СН3COOH + C2H5OH = СН3COOC2H5 + H2O,
взаимодействие ангидридов или галогенангидридов карбоновых кислот со спиртами (например, получение этилацетата из уксусного ангидрида и этилового спирта):
(CH3CO)2O + 2C2H5OH = 2 СН3COOC2H5 + H2O,
взаимодействие солей кислот с алкилгалогенидами:
RCOOMe + R'Hal = RCOOR' + MeHal.
Жиры
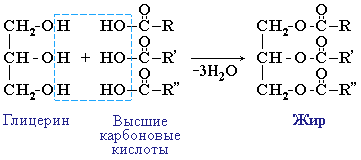
Жиры – сложные эфиры глицерина и высших одноосновных карбоновых кислот.
Номенклатура и классификация
Общее название жиров – триацилглицерины или триглицериды, ацил – остаток карбоновой кислоты –C(O)R. В природные триглицериды входят остатки в основном насыщенных (предельных) кислот (стеариновой C17H35COOH, пальмитиновой C15H31COOH, и др.), а также непредельных кислот (линолевой C17H31COOH, олеиновой C17H33COOH, линоленовой C15H29COOH и др.).
Жиры можно найти во всех животных и растениях. По составу они являются смесями полных сложных эфиров глицерина и не имеют чётко выраженной температуры плавления.
Физические свойства
Животные жиры (свиной, говяжий, бараний и т. п.) большей частью являются твердыми веществами, но с невысокой температурой плавления (исключениеием является рыбий жир – жидкость). В твёрдых жирах в основном остатки насыщенных кислот.
Растительные жиры – масла (кукурузное, подсолнечное, соевое, хлопковое и др.) – это жидкости (исключение – кокосовое масло и масло какао-бобов). Масла включают в себя остатки ненасыщенных кислот.
Жидкие жиры превращаются в твердые путем реакции гидрогенизации (гидрирования). При этом водород присоединяется по двойной связи, содержащейся в углеводородном радикале молекул масел.
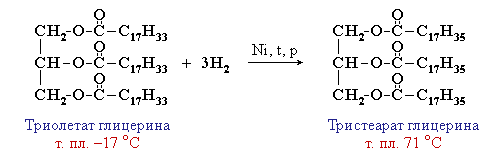
Продукт гидрогенизации масел – твердый жир (искусственное сало, саломас). Маргарин – это пищевой жир, состоящий из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкового и др.), а также животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др.).
Для жиров, как сложных эфиров, характерна обратимая реакция гидролиза (катализатор – минеральные кислоты). В присутствии щелочей (или карбонатов натрия или калия) гидролиз жиров протекает необратимо. Продуктами в этом случае являются мыла – соли высших карбоновых кислот и щелочных металлов:
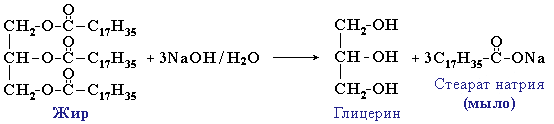
Натриевые соли – твердые мыла, калиевые – жидкие. Реакция щелочного гидролиза жиров, и вообще всех сложных эфиров, называется также омылением.
Высшие карбоновые кислоты можно выделить из мыла действием более сильных кислот.
Жиры, содержащие остатки ненасыщенных кислот, способны к окислению по связям С=С.
Важное значение имеют так называемые высыхающие масла (льняное, тунговое и др.), которые входят в состав красок и лаков (в частности, олифы). Эти масла отличаются высоким содержанием остатков кислот с двумя или тремя двойными связями и способны к образованию на окрашиваемой поверхности прочной пленки за счет полимеризации по кратным связям под действием кислорода воздуха.
Хлорангидриды
Номенклатура и классификация
Общая формула R–COCl. Названия хлорангидридов производятся от названий соответствующих кислотных остатков (ацилов) путем добавления к ним слова хлористый в начале или слова хлорид в конце.
Химические свойства
С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту:
R–CO–Cl + H2O → R–CO–OH + HCl.
Реакция с аммиаком, первичными и вторичными аминами приводит к соответствующим амидам:
R–CO–Cl + NH3 → R–CO–NH2 + HCl.
Реакцией с солями карбоновых кислот получают ангидриды карбоновых кислот
R–CO–Cl + R–CO–ONa → (R–CO)2O + NaCl.
Хлорангидриды карбоновых кислот в присутствии хлорид железа (III), хлорид алюминия вступают в реакцию с ароматическими соединениями, образуя ароматические кетоны:
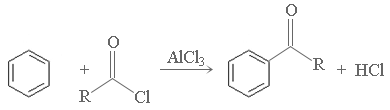
Методы получения
Получают хлорангидриды чаще всего взаимодействием безводной карбоновой кислоты с тионилхлоридом (SOCl2), трёххлористым фосфором (PCl3) или пятихлористым фосфором (PCl5), фосгеном (COCl2) [10].
R–COOH + SOCl2 → R–COCl + SO2↑ + HCl↑.
3R–COOH + PCl3 → 3R–COCl + H3PO3.
R–COOH + PCl5 → R–COCl + POCl3 + HCl.
R–COOH + COCl2 → R–COCl + CO2↑ + HCl↑.
Применение
Благодаря высокой реакционной способности, хлорангидриды широко применяются в органическом синтезе в качестве ацилирующего агента для введения в синтезируемую молекулу остатка карбоновой кислоты.
Амины
Амины – это большой класс азотсодержащих органических соединений, которые являются продуктами замещения одного, двух или трёх атомов водорода на органические радикалы R в молекуле аммиака.
Номенклатура и классификация
Добавляют слово «амин» к названию органических остатков, связанных с азотом, при этом группы упоминают в алфавитном порядке (например, CH3N(С6Н5)2 – метилдифениламин, CH3NHC3Н7 – метилпропиламин). Для высших аминов берется за основу углеводород, далее прибавляется приставка амино-, диамино-, триамино-. По числу замещенных атомов водорода различают: первичные амины – RNH2, вторичные – R2NH, третичные – R3N (где R – CH3, C3H7, C6H11, C6H5 и др.). По радикалу амины разделяют на алифатические (например, метиламин C3H7NH2, диметиламин (CH3)2NH и т. д.); алициклические (например, циклогексиламин – C6H11NH2); ароматические (например, анилин C6H5NH2) и гетероциклические (например, 2-аминопиридин C5H4N(NH2)). Амины с двумя, тремя и большим числом аминогрупп –NH2 называют ди-, три- и полиаминами (гексаметилен диамин H2N(CH2)6NH2, этилендиамин H2NCH2CH2NH2).
Строение и физические свойства
Первые представители ряда аминов – метиламин, диметиламин, триметиламин и этиламин – при комнатной температуре газы, далее при увеличении числа атомов в заместителе амины приобретают жидкое состояние, а при увеличении длины цепи до 10 атомов углерода становятся кристаллическими веществами. Растворимость аминов в воде убывает по мере увеличения длины цепи R и при возрастании числа органических групп, связанных с азотом (переход к вторичным и третичным аминам). У аминов запах схож с запахом аммиака, высшие (твердые) амины запаха не имеют.
Химические свойства
Для аминов, как и для аммиака, характерно образование донорно-акцепторной связи. Азот предоставляет неподеленную электронную пару, исполняя роль донора. В качестве акцептора электоронов может выступать, например, протон Н+, который образует ион R3NH+. Возникшая ковалентная связь N–H полностью эквивалентна остальным связям N–H в амине.
Алкиламины – сильные основания, ариламины основания слабее.
Водные растворы алифатических аминов проявляют щелочную реакцию (при их взаимодействии с водой образуются гидроксиды алкиламмония), аналогичные гидроксиду аммония:
C2H5NH2 + H2O → [C2H5NH3]+ + OH−.
Взаимодействуя с кислотами, амины образуют алкиламиновые соли, в большинстве случаев растворимые в воде. Например, амины присоединяют галогеноводороды:
RNH2 + HCl → [RNH3]Cl−.
Амины присоединяют галогеналканы RCl с образованием донорно-акцепторной связи N–R, которая также эквивалентна уже имеющимся.
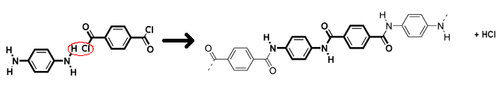
При нагревании с карбоновыми кислотами, их ангидридами, хлорангидридами или сложными эфирами первичные и вторичные амины ацилируются с образованием N-замещенных амидов, соединений с фрагментом –С(О)N<:

Реакция с ангидридами проходит в мягких условиях. Хлорангидириды реагируют ещё легче, реакция проходит в присутствии основания, чтобы связать образующийся хлороводород.
При введении в реакцию диамина и дикарбоновой кислоты, они взаимодействуют по той же схеме, но так как каждое соединение имеет две функциональные группы, то образуется полиамид.
Первичные и вторичные амины реагируют с азотистой кислотой по-разному и при помощи HNO2 первичные, вторичные и третичные амины различают. Из первичных аминов получаются первичные спирты:
C2H5NH2 + HNO2 → C2H5OH + N2 + H2O.
При этом выделяется газ (азот). Это признак того, что в колбе первичный амин.
Вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины – соединения, содержащие фрагмент >N–N=O:
(C2H5)2NH + HNO2 → (C2H5)2N–N=O + H2O.
Вторичные амины легко узнать по запаху нитрозодиметиламина.
Третичные амины при нормальной температуре в азотистой кислоте растворяются.
Конденсация первичных аминов с альдегидами и кетонами приводит к образованию аминов или так называемых оснований Шиффа – соединений, содержащих фрагмент –N=C<:
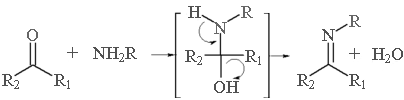
Методы получения
В аминах атом азота находится в наименьшей степени окисления, поэтому многие способы их получения связаны с восстановлением азотсодержащих соединений (например, нитропроизводных углеводородов, амидов, нитрилов).
Общим методом получения первичных аминов считается восстановление нитросоединений:
R–NO2 ![]() R–NH2.
R–NH2.
Анилин – важнейший ароматический амин, который образуется при восстановлении нитробензола (восстановителем является водород в присутствии металлических катализаторов, а также, например, сульфиды):
C6H5NO2 + 6[H] → C6H5NH2 + 2H2O.
Эта реакция носит имя химика Н. Н. Зинина, осуществившего ее впервые в 1842 г.
Восстановление амидов (восстановитель – алюмогидрид лития):
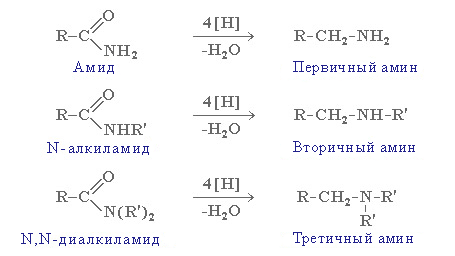
Восстановление нитрилов с образованием первичных аминов:
R–CN + 4[H] = R–CH2NH2
Этим способом в промышленности получают гексаметилендиамин, который используется в производстве полиамидного волокна найлон.
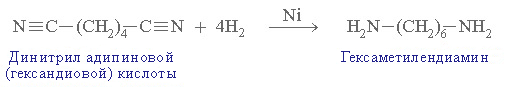
Получение аминов путём введения алкильных групп в молекулы аммиака и аминов (реакции алкилирования).
При нагревании галогеналканов с аммиаком образуется смесь первичных, вторичных и третичных аминов:
NH3 + CH3Cl → [CH3NH3]+Cl– ![]() CH3NH2 + NH4Cl
CH3NH2 + NH4Cl
CH3NH2 + CH3Cl → [(CH3)2NH2]+Cl– ![]() (CH3)2NH + NH4Cl
(CH3)2NH + NH4Cl
(CH3)2NH + CH3Cl → [(CH3)3NH]+Cl– ![]() (CH3)3N + NH4Cl
(CH3)3N + NH4Cl
Применение
Амины применяются мало в виде отдельных соединений. Например, в быту используется полиэтиленполиамин [–C2H4NH–]n (торговое название ПЭПА) в качестве отвердителя эпоксидных смол. Основное применение аминов – промежуточные продукты для получения других органических веществ. Чаще всего используется анилин, так как на его основе производится широкий спектр анилиновых красителей (Бриллиантовый зелёный, Метиленовый синий, мовеин, анилиновый чёрный, голубой, жёлтый, оранжевый). Алифатические диамины – исходные вещества для синтеза полиамидов, например, нейлона, используемого для изготовления волокон и пленок.
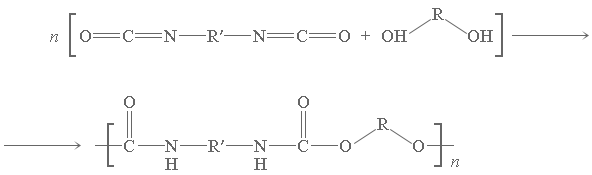
Из алифатических диизоцианатов получают полиуретаны, которые обладают комплексом технически важных свойств: высокой прочностью в сочетании с эластичностью и очень высоким сопротивлением истиранию (полиуретановые обувные подошвы), а также хорошей адгезией к широкому кругу материалов (полиуретановые клеи). Широко их применяют и во вспененной форме (пенополиуретаны).
Из сульфаниловой кислоты NH2–C6H4–SO3H получают противовоспалительные лекарственные препараты.
Соли диазония 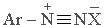 применяют в фоточувствительных материалах для копирования, которое позволяет получать изображение без процедур, характерных для фотографии.
применяют в фоточувствительных материалах для копирования, которое позволяет получать изображение без процедур, характерных для фотографии.
Аминокислоты
Аминокислоты (аминокарбоновые кислоты) – органические соединения, в молекуле которых одновременно содержатся аминные и карбоксильные группы.
Номенклатура и классификация
По систематической номенклатуре названия аминокислоты образуют по названию соответствующей кислоты прибавлением приставки амино- и указанием расположения аминогруппы к карбоксильной группе.
Например:
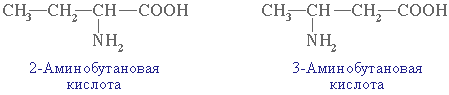
Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Например:
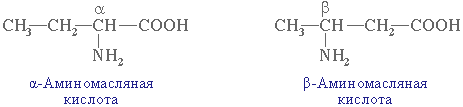
Для α-аминокислот R–CH(NH2)COOH, которые играют исключительно важную роль в процессах жизнедеятельности животных и растений, применяются тривиальные названия.
Некоторые важнейшие α-аминокислоты
| Формула | Название | Обозначение |
|---|---|---|
| H2N–Ch2–COOH | Глицин | Gly (Гли) |
| CH3–CH(NH2)–COOH | Аланин | Ala (Ала) |
| C6H5CH2–CH(NH2)–COOH | Фенилаланин | Phe (Фен) |
| (CH3)2CH–CH(NH2)–COOH | Валин | Val (Вал) |
| (CH3)2CH–CH2–CH(NH2)–COOH | Лейцин | Leu (Лей) |
| HOCH2–CH(NH2)–COOH | Серин | Ser (Сер) |
| H2N–CO–CH2–CH(NH2)–COOH | Аспарагин | Asn (Асн) |
В зависимости от природы кислотной функции аминокислоты подразделяют на аминокарбоновые (например, H2N(CH2)5COOH), аминосульфоновые (например, H2N(CH2)2SO3H), аминофосфоновые (например, H2NCH[Р(О)(ОН)2]2) и аминоарсиновые (например, H2NC6H4AsO3H2).
По способности человека синтезировать их из предшественников: на незаменимые (триптофан, лизин, фенилаланин, метионин, треонин, валин, лейцин, изолейцин, аргинин, гистидин) и заменимые (глутамин, аспарагиновая кислота, тирозин, цистеин, глицин, глутаминоваякислота, аланин, серин, аспарагин, пролин).
По функциональным группам аминокислоты бывают: алифатические, ароматические, гетероциклические.
Аминокислоты классифицируют по двум структурным признакам.
В зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты подразделяют на α–, β–, γ–, δ–, ε– и т. д.
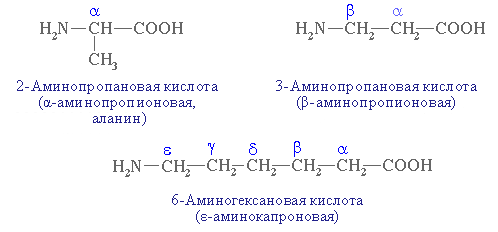
Строение и физические свойства
Аминокислоты резко отличаются от соответствующих кислот и оснований по физическим и ряду химических свойств. Они хорошо растворимы в воде, но плохо в органических растворителях; хорошо кристаллизуются; имеют высокую плотность и очень высокие температуры плавления (иногда разлагаются). Эти свойства обусловлены взаимодействием аминных и кислотных групп, вследствие чего аминокислоты в твердом состоянии и в растворе (в широком интервале рН) находятся в цвиттер-ионной форме. Взаимное влияние групп особенно сильно проявляется у α-аминокислот, в которых обе группы находятся у соседних атомов углерода. Также у o- и π-аминобензойных кислот наблюдается аналогичный эффект, где их взаимодействие передается через систему сопряженных связей. Благодаря электроноакцепторным свойствам группы –NН3+, заметно повышается кислотность карбоксильных групп (например, рКа глицина 2,34, а уксусной кислоты 4,75).
Аминогруппа подвергается влиянию электроноакцепторной карбонильной группы и электронодонорного отрицательно заряженного атома кислорода, в результате чего, например, основность аминогрупп аминоуксусной и π-аминобензойной кислот мало отличается от основности соответственно этиламина и анилина. Аминогруппа аминокислоты ионизирована в несколько меньшей степени, чем карбоксильная группа, а водный раствор аминокислоты имеет слабокислый характер. Значение рН, при котором концентрация катионов аминокислоты равна концентрации анионов, называется изоэлектрической точкой (рI). Все аминокислоты в изоэлектрической точке имеют минимум растворимости (в растворах кислот и щелочей растворимость возрастает). Вблизи рI растворы аминокислоты обладают минимальным буферным действием, а вблизи рК каждой функциональной группы – максимальным.
Химические свойства
Аминокислоты проявляют свойства оснований за счет аминогруппы и свойства кислот за счет карбоксильной группы, т. е. являются амфотерными соединениями. Подобно аминам, они реагируют с кислотами с образованием солей аммония:
H2N–CH2–COOH + HCl [H3N+–CH2–COOH]Cl–.
Как карбоновые кислоты они образуют функциональные производные:
a) соли
H2N–CH2–COOH + NaOH → H2N–CH2–COO–Na+ + H2O;
б) сложные эфиры.
Кроме того, возможно взаимодействие амино- и карбоксильной групп как внутри одной молекулы (внутримолекулярная реакция), так и принадлежащих разным молекулам (межмолекулярная реакция).
Практическое значение имеет внутримолекулярное взаимодействие функциональных групп ε-аминокапроновой кислоты, в результате которого образуется ε-капролактам (полупродукт для получения капрона):

Межмолекулярное взаимодействие α-аминокислот приводит к образованию пептидов. При взаимодействии двух α-аминокислот образуется дипептид.
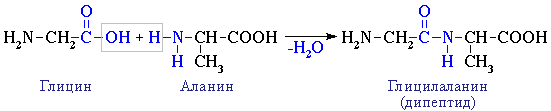
Межмолекулярная реакция с участием трех α-аминокислот приводит к образованию трипептида и т. д.
Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH – пептидной связью.
Важнейшие природные полимеры – белки, которые относятся к полипептидам, т. е. представляют собой продукт поликонденсации α-аминокислот:
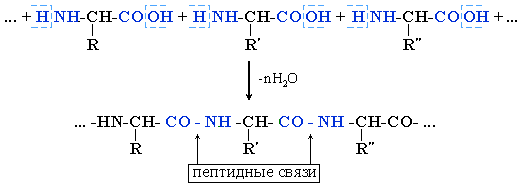
Методы получения
1.Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах.
2.Присоединение аммиака к α-, β-непредельным кислотам с образованием β-аминокислот:
CH2=CH–COOH + NH3 = H2N–CH2–CH2–COOH.
3.α-аминокислоты образуются при гидролизе пептидов и белков.
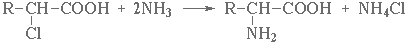
4.Восстановление нитрозамещенных карбоновых кислот (применяется обычно для получения ароматических аминокислот):
O2N–C6H4–COOH + 3H2 = H2N–C6H4–COOH + 2H2O.
5.Биотехнологический способ получения чистых α-аминокислот в виде индивидуальных оптических изомеров. Этот способ основан на способности специальных микроорганизмов вырабатывать в питательной среде определенную аминокислоту.
Применение
Наибольший интерес представляют 20 L-α-аминокислот (аланин, аргинин, аспарагин и другие), входящих в состав белковых молекул. Смеси L-аминокислот, а также индивидуальные аминокислоты (например, метионин) применяют в медицине для парэнтерального питания больных с заболеваниями пищеварительных и других органов, при нарушениях обмена веществ и др.; лизин, метионин, треонин, триптофан – в животноводстве для обогащения кормов; глутамат натрия и лизин – в пищевой промышленности. ω-аминокислоты и их лактамы служат для промышленного производства полиамидов. γ-аминомасляная кислота (аминалон) – медиатор в центральной нервной системе, применяется как лекарственное средствово при сосудистых заболеваниях головного мозга. Ароматические аминокислоты используют в синтезе красителей и лекарственных средств. На основе аминокарбоновых и аминофосфоновых кислот синтезируют селективные комплексоны, комплексообразующие иониты, лигандообменные сорбенты, ПАВ.